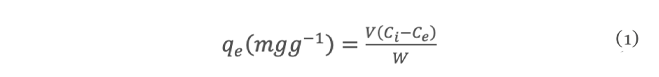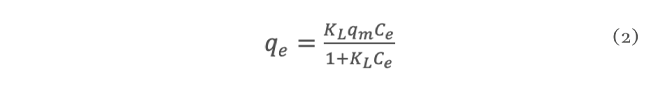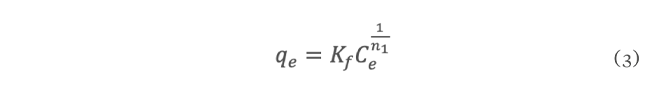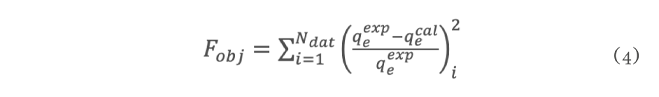Adsorción de iones de Pb2+ empleando CaCO3 biogénico en soluciones acuosas
Adsorption of Pb2+ ions using biogenic CaCO3 in aqueous solutions
 https://orcid.org/0000-0002-1509-8632
https://orcid.org/0000-0002-1509-8632
Laura Lorena Díaz Flores División Académica de Ingeniería y Arquitectura. Universidad Juárez Autónoma de Tabasco Laura.flores@ujat.mx
 https://orcid.org/0000-0002-0415-3093
https://orcid.org/0000-0002-0415-3093
María de los Ángeles Olan Acosta División Académica de Ingeniería y Arquitectura. Universidad Juárez Autónoma de Tabasco maria.olan@ujat.mx
 https://orcid.org/0000-0002-8446-1650
https://orcid.org/0000-0002-8446-1650
Manuel Olán Ramos Tecnológico Nacional de México Campus Comalcalco. Comalcalco Tabasco, México manuel.olan@comalcalco.tecnm.mx
 https://orcid.org/0000-0001-9980-9165
https://orcid.org/0000-0001-9980-9165
Rafael Valenzuela Rodríguez Tecnológico Nacional de México Campus Comalcalco. Comalcalco Tabasco, México rafael.valenzuela@comalcalco.tecnm.mx
 https://orcid.org/0000-0002-8114-465X
https://orcid.org/0000-0002-8114-465X
DOI: https://doi.org/10.31644/IMASD.32.2023.a05
Fecha de recepción: 11 de julio 2022
Fecha de aceptación: 28 de septiembre 2022
Fecha de publicación: 01 de febrero 2023
Resumen
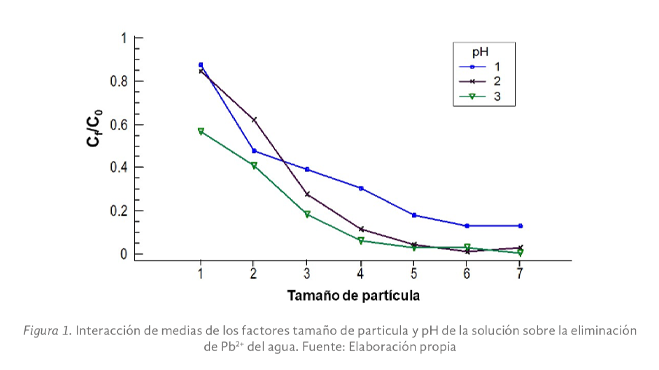
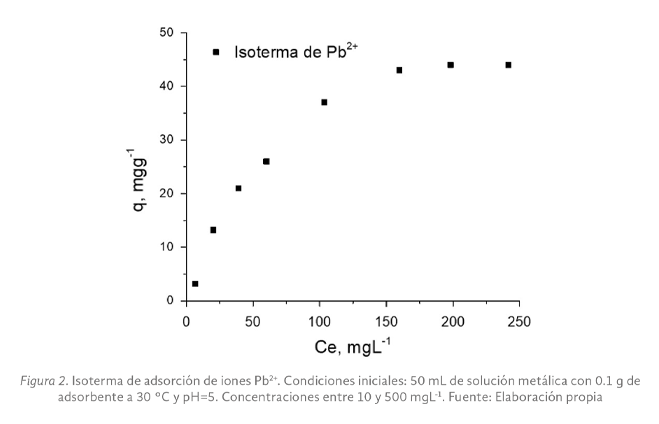
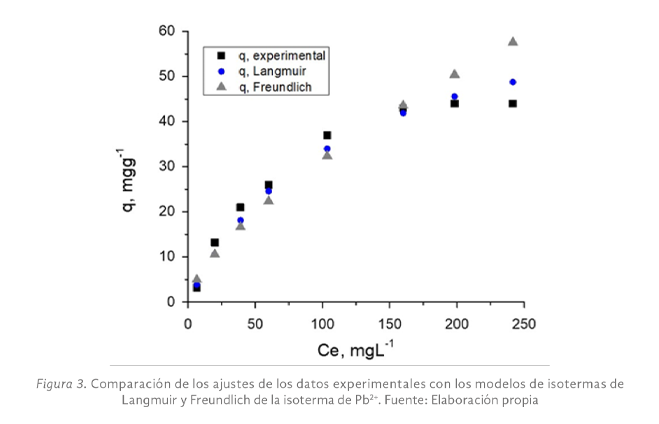
En el estado de Tabasco se cultiva el ostión Crassostrea Virginica, esta producción lo convierte en una importante actividad económica y de manera adversa en un foco de infección por los desechos de la parte no comestible. Sin embargo, estas valvas están compuestas por CaCO3 con potencial aplicación como adsorbentes de metales pesados disueltos en agua y así mejorar la calidad de esta. En esta investigación se empleó un adsorbente de CaCO3 obtenido de conchas de ostión para la eliminación de plomo (Pb2+) del agua. Las valvas fueron lavadas y secadas al sol, posteriormente se trituraron con martillo para ingresarlas a un molino de alta energía y reducir su tamaño. Los polvos se tamizaron en mallas #100, #200 y lo que pasa la #200 y los valores de pH de la solución de plomo se ajustaron en función al diagrama de especie del metal para tenerlo en solución e identificar las mejores condiciones de experimentación. Los resultados mostraron que a condiciones de pH=5 y tamaños de partículas del orden de 0.074 mm se obtuvieron los mejores resultados. Con estas condiciones se procedió a obtener las isotermas de adsorción y se obtuvieron capacidades máximas de adsorción de 44 mgg-1 del ion Pb2+.
Palabras clave: Adsorción; Iones metálicos; Carbonato de calcio; Biogénico.
-Abstract-
In the state of Tabasco, the oyster Crassostrea Virginica is cultivated, this production makes it an important economic activity and adversely in a source of infection by the waste of the inedible part. However, these leaflets are composed of CaCO3 with potential application as adsorbents for heavy metals dissolved in water and thus improve its quality. In this research, a CaCO3 adsorbent obtained from oyster shells was used to remove lead (Pb2+) from water. The shells were washed and dried in the sun, later they were crushed with a hammer to enter them in a high-energy mill and reduce their size. The powders were sieved in meshes #100, #200 and what happens to #200 and the pH values of the lead solution were adjusted according to the metal species diagram to keep it in solution and identify the best experimental conditions. The best results were obtained under conditions of pH=5 and particle sizes of the order of 0.074 mm. With these conditions, the adsorption isotherms were obtained and maximum adsorption capacities of 44 mgg-1 of the Pb2+ ion were obtained.
Keywords: Adsorption; metal ions; calcium carbonate; biogenic.