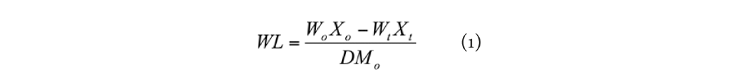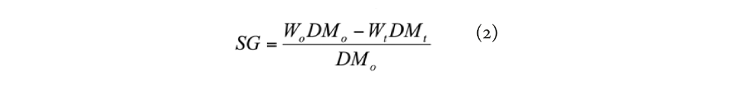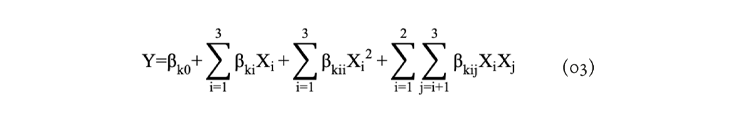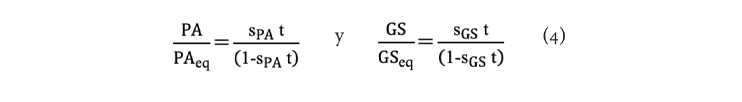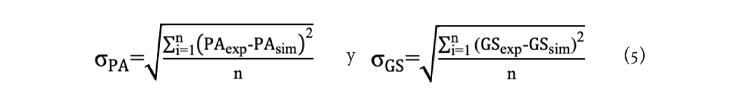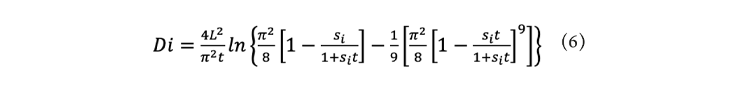Introducción
En México, la producción anual de mango (Mangifera indica) en 2023 fue de más de dos millones de toneladas, Sinaloa, Guerrero, Nayarit, Chiapas y Oaxaca fueron los estados mayores productores (Smattcom, 2024). A pesar de que cerca de 20 % de la producción se destinó en 2017 para su exportación a Estados Unidos y otros países (SAGARPA, 2017), el resto fue comercializado en el país en forma de fruta fresca o procesada como jugos, néctares, así como productos deshidratados. Las variedades Tommy Atkins, Ataulfo y Kent han sido ampliamente estudiadas, sin embargo, existe poca información científica y tecnológica de la variedad Oro, por lo que es importante generar información científica y tecnológica.
En este contexto, la deshidratación es un proceso que permite la eliminación del agua con el propósito de obtener productos con bajo contenido de humedad, lo que favorece una vida en anaquel superior a la de un producto fresco (Kilic et al., 2023). No obstante, las propiedades fisicoquímicas y sensoriales del producto pueden variar drásticamente. Kilic et al. (2023) reportaron una revisión sobre los diferentes métodos de secado. En este trabajo, estos autores mencionan que la deshidratación con aire caliente permite obtener productos con larga vida en anaquel, pero las características sensoriales y nutrimentales de los productos podrían disminuir drásticamente. Estos autores también reportan que existen otros métodos como la deshidratación osmótica (DO), que permite la obtención de alimentos con mejores características sensoriales que los alimentos deshidratados (Kilic et al., 2023). Por esta razón, la deshidratación osmótica es un proceso ampliamente utilizado para incrementar la vida en anaquel de los alimentos (Marie et al., 2025).
La DO es una técnica de procesamiento que consiste en la inmersión de matrices alimentarias en una solución con elevada concentración de solutos (Asghari et al., 2024) y que conlleva tres etapas: i) la transferencia de agua del producto a la solución hipertónica, ii) la migración del soluto osmótico al producto; y iii) la lixiviación de componentes de la matriz natural (azúcares, ácidos, minerales, vitaminas) en la solución hipertónica (Huerta-Vera et al., 2024). La DO ha sido estudiada por muchos autores encontrando que la concentración de solutos (Arias et al., 2017), la temperatura de la solución osmótica (Arias et al., 2017), la presión a la cual se efectúa el proceso (Vinod et al., 2024; Staniszewska et al., 2024), la relación jarabe:fruta (Vinod et al., 2024) y el tiempo de proceso (Vinod et al., 2024), influyen en la pérdida de agua y ganancia de solutos. La DO se ha utilizado para la conservación de diferentes frutas, incluyendo el mango. Arias et al. (2017) estudiaron la cinética de transferencia de masa durante la deshidratación osmótica de láminas de mango (Mangifera indica L.) var. Tommy Atkins en soluciones de sacarosa (45-60 °Brix) a diferentes temperaturas (20, 35 y 50 ºC) durante 6 h. Sin embargo, estos autores utilizaron una relación jarabe/fruta (mL:g) de 3:1, lo cual podría diluir a la solución después de la primera hora de proceso, provocando cambios en la concentración de la solución osmótica de tal forma que la transferencia de masa no fue constante.
La metodología de superficie de respuesta ha sido empleada para optimizar procesos de DO en frutas, según lo reportaron Tsopwo Zena y Jiokap Nono (2024). No obstante, los coeficientes de determinación obtenidos mediante regresión múltiple no siempre presentan niveles de ajuste satisfactorios. En consecuencia, diversos investigadores han recurrido a modelos matemáticos alternativos, tales como los propuestos por Azuara, Peleg y Weibull, los cuales han demostrado mayor capacidad para describir la cinética de pérdida de agua y ganancia de solutos durante la DO, así como para estimar la difusividad efectiva de dichos fenómenos (Sulistyawati et al., 2020). La determinación de las difusividades efectivas de agua y solutos en la deshidratación osmótica permite predecir con mayor precisión la evolución del contenido de humedad y sólidos en el producto tratado y optimizar las condiciones del proceso.
A pesar de que existen diversas publicaciones sobre la DO de mango, a nuestro conocimiento pocos trabajos se han publicado sobre la variedad Oro. Por lo que en este trabajo se determinó el efecto de la concentración de sacarosa (40 y 60 °Brix) y de la temperatura (40 y 60 °C) de la solución osmótica, así como la aplicación de un pulso de vacío (5 y 15 lb/plg2) sobre la pérdida de agua (PA) y ganancia de solutos (GS) de mango (Mangifera indica var. Oro) y el grado de aceptación del mango osmodeshidratado. Además, la PA y GS se modelaron para el cálculo de las difusividades efectivas del agua y de la sacarosa durante la deshidratación osmótica.
Materiales y métodos
Deshidratación osmótica
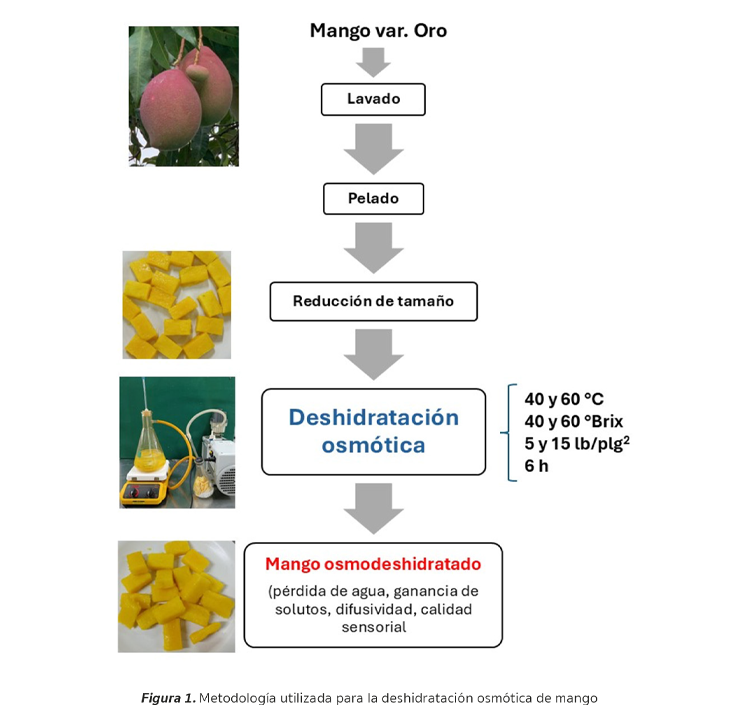
Los frutos de Mangifera indica var. Oro se obtuvieron de un supermercado local en la ciudad de Tuxtla Gutiérrez, Chiapas, México. Los mangos se lavaron y pelaron manualmente y se prepararon cortes en forma de paralelepípedos rectangulares de 30 mm de largo, 18 mm de ancho y 10 mm de espesor. Los trozos se sumergieron en una solución de sacarosa comercial a concentración y temperatura controladas. La Figura 1 muestra la metodología utilizada para la deshidratación osmótica de mango.
Aproximadamente 100 g de mango se sumergieron en 1 kg de solución osmótica a temperatura controlada en un matraz Erlenmeyer equipado con agitación magnética y un tapón que contenía un tubo para hacer vacío, según lo reportado por Grajales-Lagunes et al. (2019). Esta relación fruta:solución osmótica de 1:10 (p:p) fue para evitar la dilución de la solución osmótica (Antonio et al., 2008). En los primeros diez minutos de la DO, se aplicó el pulso de vacío (VP) y posteriormente se restableció la presión atmosférica, como lo describen Grajales-Lagunes et al. (2019). Las muestras de mango se tomaron a los 0, 10 y 360 min, posteriormente, se lavaron con agua destilada para eliminar la sacarosa superficial y luego se limpiaron con papel absorbente. Las muestras se pesaron en balanza analítica (Ohaus, New Jersey, EE. UU.) (sensibilidad de 0.0001 g) y se determinó el contenido de humedad por quintuplicado en un horno de vacío a 60 °C hasta peso constante.
La PA y la GS se calcularon utilizando las ecuaciones 1 y 2:
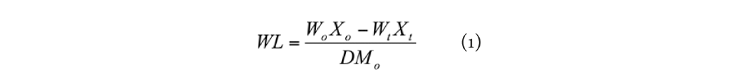
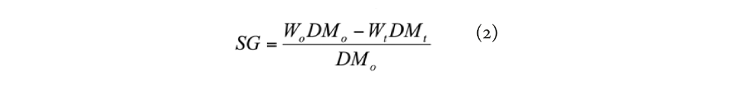
Donde Wo es el peso del mango (g), Xo es el contenido de humedad (g g-1), DMo es la fracción de materia seca (g g-1) al comienzo del secado osmótico, y Wt, Xt y DMt los valores correspondientes durante el secado osmótico.
Diseño experimental y análisis estadístico
Se empleó un diseño experimental de superficie de respuesta tipo Box-Behnken, con cada tratamiento realizado por triplicado y tres repeticiones adicionales en el punto central, lo que resultó en un total de 13 tratamientos (Tabla 1). Se evaluó el efecto de la temperatura (40 y 60 °C), el contenido de sacarosa (40 y 60 °Brix) y el pulso de vacío (5 y 15 lb/plg2) sobre la PA y GS de trozos de mango durante el secado osmótico. El análisis de resultados se realizó con ayuda del programa Statgraphics Centurion XV (StatPoint Technologies, Inc., Virginia, EE. UU.). La PA y GS fueron modelados mediante la metodología de superficie de respuesta (Tsopwo Zena y Jiokap Nono, 2024) con ayuda de la ecuación 3:
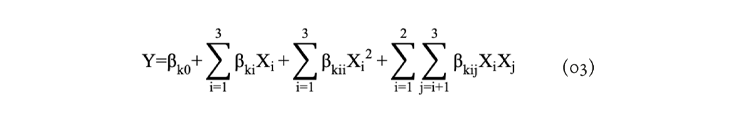
Donde Y denota la ganancia de solutos o pérdida de agua; βk0, βki, βkii and βkij son los coeficientes del modelo; y Xi y Xj son las variables independientes no codificadas. El R2 para cada ecuación fue calculado y reportado.
Además, la PA y GS fueron ajustados con el modelo reportado por Azuara (Sulistyawati et al. 2020):
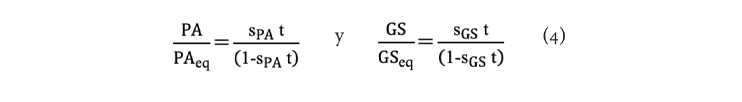
Donde PAeq y GSeq son la PA y la GS después de 6 horas, sPA y sGS son las constantes empíricas por identificar y t es el tiempo en horas. PAeq y GSeq son las pérdidas de agua y ganancia de solutos en el equilibrio y sPA y sGS son las constantes empíricas por identificar. Estas constantes fueron calculadas empleando los promedios de la cinética de deshidratación osmótica utilizando el método Simplex-modificado (Jarry-Bolduc y Planiden, 2025) mediante la minimización de las funciones objetivas representadas en las ecuaciones 5.
Los valores de sPA y sGS fueron calculados para cada tratamiento:
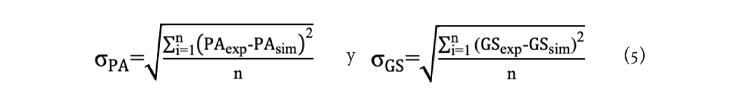
Donde n representa el número total de datos experimentales, y los subíndices exp y sim indican los valores experimentales y simulados, respectivamente.
La difusividad del agua y de la sacarosa (Di), en función de s, fue calculada mediante la ecuación 6:
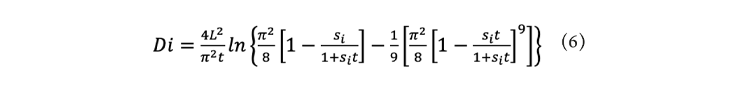
Donde L corresponde a la mitad del espesor de la muestra en milímetros, t es el tiempo en segundos y si las constantes a identificar para la PA y GS.
Análisis sensorial
Después de seis horas de secado osmótico, las muestras de mango se analizaron mediante una prueba hedónica estructurada de 9 puntos aplicada a 100 jueces no entrenados (D´Aquino de los Santos et al., 2022). Los análisis sensoriales de los 12 tratamientos fueron realizados en sesiones independientes. En cada sesión de evaluación sensorial, cada juez calificó la aceptación global de las muestras de mango correspondientes a cuatro tratamientos, con el fin de evitar la fatiga sensorial. La muestra estuvo conformada por 100 jueces no entrenados (46 hombres y 54 mujeres), con edades comprendidas entre los 18 y 25 años. Todos los participantes fueron informados de que podían abandonar la prueba en cualquier momento si así lo deseaban. Los resultados se analizaron mediante la prueba de Tukey, considerando un nivel de significancia de p < 0.05.
RESULTADOS Y DISCUSIONES
Pérdida de agua y ganancia de solutos
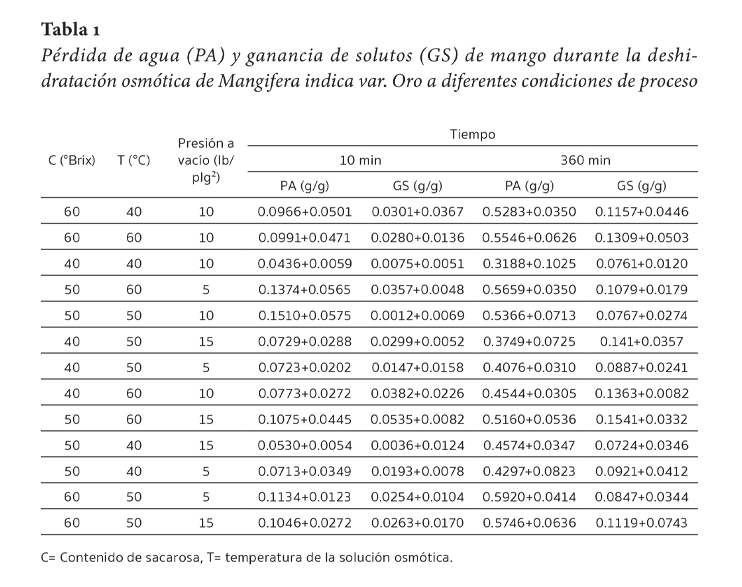
Los resultados mostraron que el mango pierde agua y se impregna de sacarosa durante la DO (Tabla 1). Estos resultados coinciden con lo reportado por Sulistyawati et al. (2020) y Tsopwo Zena y Jiokap Nono (2024).
A los 10 minutos de tratamiento, la pérdida de agua osciló entre 0.0436 y 0.1510 g de agua/g de fruta fresca, mientras que la ganancia de solutos se ubicó entre 0.0012 y 0.0535 g de sacarosa/g de fruta fresca. En contraste, tras 360 minutos de tratamiento, la pérdida de agua varió entre 0.3188 y 0.5920 g de agua/g de fruta fresca, y la ganancia de solutos entre 0.0724 y 0.1541 g de sacarosa/g de fruta fresca.
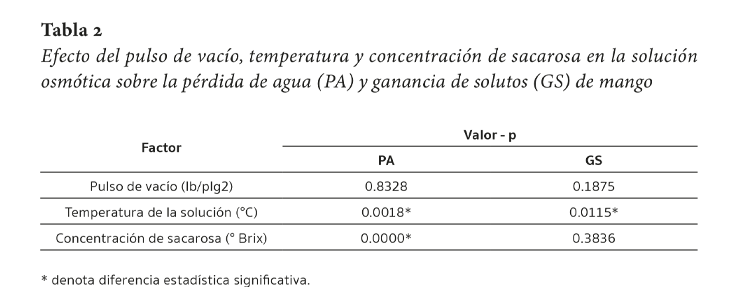
La concentración de sacarosa y la temperatura de la solución tuvieron efecto estadístico significativo sobre la pérdida de agua (Tabla 2). Estos resultados coinciden con Sablani y Rahman (2003), quienes exponen que la pérdida de agua aumenta con el incremento de la temperatura y de la concentración. De la misma forma, Zapata Montoya y Montoya Rodas (2012) reportaron que la temperatura de la solución afectó la transferencia de masa durante la deshidratación osmótica de mango Tommy Atkins. Sin embargo, el pulso de vacío no tuvo efecto estadístico significativo. Esto debido probablemente a la baja porosidad del mango, la cual no permitió el intercambio de soluto de la solución a la fruta según lo informaron Mújica-Paz et al. (2003).
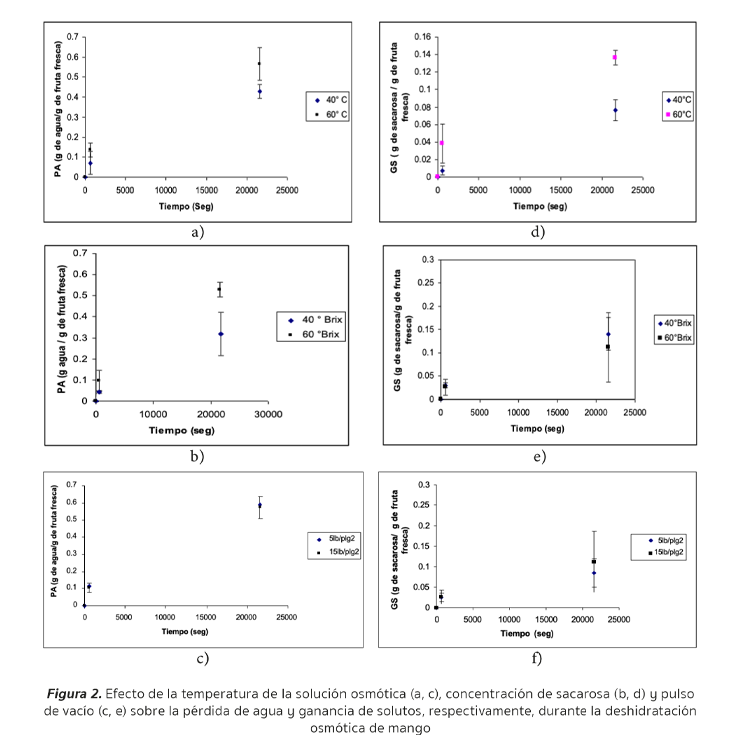
La PA y GS incrementaron con la temperatura de la solución osmótica después de 6 h de secado, pero este efecto no fue significativo en los primeros 10 min (Figura 2). La Figura 2c muestra que la aplicación del pulso de vacío no influyó en la PA ni GS. Los resultados en este estudio difieren de los reportados por Lin et al. (2016) y Sulistyawati et al. (2018), quienes observaron que la aplicación de pulsos de vacío sí influía en la transferencia de masa durante la deshidratación osmótica de mango. Esta discrepancia podría atribuirse, al menos en parte, a las diferencias metodológicas en la forma de aplicar el vacío. En particular, Sulistyawati et al. (2018) señalaron que el pulso de vacío tuvo un efecto negativo sobre la pérdida de agua, pero favoreció la ganancia de solutos. Por el contrario, Lin et al. (2016) demostraron que la aplicación de vacío facilitó tanto la pérdida de agua como la incorporación de solutos. Estas divergencias sugieren que el impacto del vacío sobre los mecanismos de transferencia de masa puede depender críticamente de variables operativas específicas, como la duración, intensidad y secuencia de los pulsos aplicados, así como de las características fisicoquímicas del sistema alimentario tratado.
El análisis de varianza mostró que la temperatura tuvo efecto significativo sobre la GS (Tabla 2). Este hecho se muestra claramente en la Figura 2d, en la cual al incrementar la temperatura aumenta la ganancia de solutos. Los resultados anteriores concuerdan con lo reportado por Sablani y Rahman (2003), quienes indicaron que la ganancia de solutos incrementa con la temperatura de la solución. Sin embargo, estos resultados difieren con lo reportado por Gomes-Corrêa et al. (2016) quienes demostraron que el pulso de vacío disminuyó la ganancia de solutos durante la DO de tomate. Estas discrepancias podrían ser explicadas por las diferencias en la composición y estructura del mango y el tomate.
Análisis sensorial
La PA y GS del mango durante la DO pudo haber modificado la aceptación global del producto. En ese sentido, la prueba hedónica mostró que las condiciones del procesamiento tuvieron un efecto estadístico significativo sobre la aceptación global del mango “Oro” (Tabla 3). Las muestras que tuvieron mayor y menor grado de aceptación ante los jueces no entrenados fueron la muestra I tratada a 50 °Brix, 60 °C y 15 lb/plg2 y la muestra C tratada a 40 °Brix, 40 °C y 10 lb/plg2, respectivamente. La muestra I obtuvo una calificación de 7.38 (me gusta moderadamente) mientras que la muestra C obtuvo 6.01 (me gusta un poco). Es de gran interés el hecho de que todas las muestras presentaron un grado de aceptación global (en la escala verbal) mayor a “me gusta” por lo que consideramos que cualquier condición de procesamiento podría ser utilizadas para fines industriales.
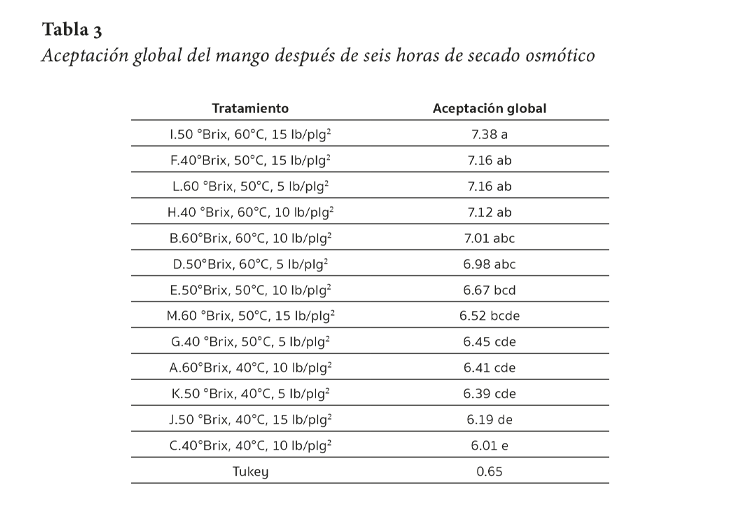
Pocos trabajos han reportado el grado de aceptación del mango osmodeshidratado. En ese contexto, la deshidratación osmótica como pretratamiento del mango previo al secado con aire caliente mejoró las propiedades sensoriales según lo reportado por Sanjinez-Argandoña et al. (2017). Además, Zapata Montoya y Montoya Rodas (2012) reportaron que el análisis sensorial efectuado en láminas de mango cv. Tommy Atkins arrojó 100 % de aceptación para las muestras de láminas de mango osmodeshidratado a 45 °C y 3 % de ácido cítrico en la solución osmótica. Sin embargo, a diferencia de este trabajo, estos autores no detallaron la prueba utilizada. Sin embargo, estos valores son superiores a los reportados por Bernardi et al. (2009) para mango osmodeshidratado con valores máximos de 5.69 para la escala hedónica de nueve puntos.
Desde una perspectiva reflexiva sobre los costos asociados al proceso de deshidratación osmótica de mango, y considerando el nivel de aceptación global alcanzado por los productos obtenidos en este trabajo, se propone la implementación de condiciones operativas más eficientes: temperaturas reducidas, bajas concentraciones de sacarosa y la omisión del pulso de vacío. Esta estrategia permitiría obtener productos sensorialmente aceptables, al tiempo que contribuiría a la disminución de los costos de producción. En particular, la reducción de la temperatura y de la concentración de sacarosa, junto con la eliminación del tratamiento por vacío, implican menores requerimientos energéticos y de insumos. No obstante, para validar la viabilidad de esta propuesta, resulta indispensable llevar a cabo un estudio técnico-económico que cuantifique los beneficios potenciales y evalúe su aplicabilidad a escala industrial.
Optimización del proceso de deshidratación osmótica
Para optimizar el proceso de DO para el mango, se utilizó la metodología de superficie de respuesta, para lo cual se decidió maximizar la pérdida de agua y disminuir la ganancia de solutos, buscando un producto con el mejor grado de aceptación.
La primera aproximación que realizamos fue el uso de una regresión múltiple con ayuda de la metodología de superficie de respuesta. En la Tabla 4 se muestran los modelos que explican la pérdida de agua y ganancia de solutos del mango después de 6 horas de deshidratación osmótica. Es de observar que los coeficientes de determinación de los modelos (R2) no son cercanos a la unidad, por lo que la transferencia de masa (agua y sacarosa) no puede ser completamente explicada por este modelo de regresión múltiple.

Sin embargo, la metodología de superficie de respuesta demostró que la máxima pérdida de agua que puede ser obtenida es utilizando una concentración de jarabe de 60 °Brix, una temperatura de 56.67 °C y 5 lb/plg2 de presión. Esta pérdida de agua simulada por el modelo corresponde hasta 0.5912 g de agua / g de fruta fresca. Asimismo, con la metodología superficie de respuesta se encontró que la mínima ganancia de solutos que puede ser obtenida es utilizando una concentración de la solución osmótica de 47.08 °Brix, una temperatura de 43.73° C y 8.42 lb/plg2 de presión. Esta ganancia de solutos simulada por el modelo corresponde hasta 0.0745 g de agua / g de fruta fresca.
Zapata Montoya y Montoya Rodas (2012) reportaron la misma tendencia en cuanto a los coeficientes de determinación de los modelos matemáticos para la deshidratación osmótica de mango Tommy Atkins. Estos autores reportaron un coeficiente de determinación para la pérdida de agua de 0.99, pero para la ganancia de solutos fue de 0.30, siendo la ganancia de solutos la de mayor variabilidad. Lo anterior podría deberse a que durante la DO no solo sacarosa entra a la fruta, pero también se lixivian otros azúcares y compuestos solubles de la fruta a la solución, como por ejemplo los ácidos orgánicos. Aunado a lo anterior, la diferencia podría deberse a la composición y estructura de las variedades de mango utilizadas.
Al comparar los resultados del tratamiento óptimo para maximizar la pérdida de agua y minimizar la ganancia de solutos con el mejor tratamiento de evaluación sensorial, observamos que la PA y GS del tratamiento a 60 °Brix, 50 °C y 5 lb/plg2 fueron de 0.5920 y 0.0847 g / g de fruta fresca, respectivamente. Este tratamiento resulta ser semejante al tratamiento óptimo, el cual provocó una PA y una GS de 0.5938 y 0.0745 g / g de fruta fresca, respectivamente. A pesar de que los tratamientos óptimos fueron identificados mediante la metodología de superficie de respuesta, es necesario mejorar el modelo debido a los bajos coeficientes de determinación (R2), por lo que aplicamos el modelo de Azuara.
Modelo de Azuara
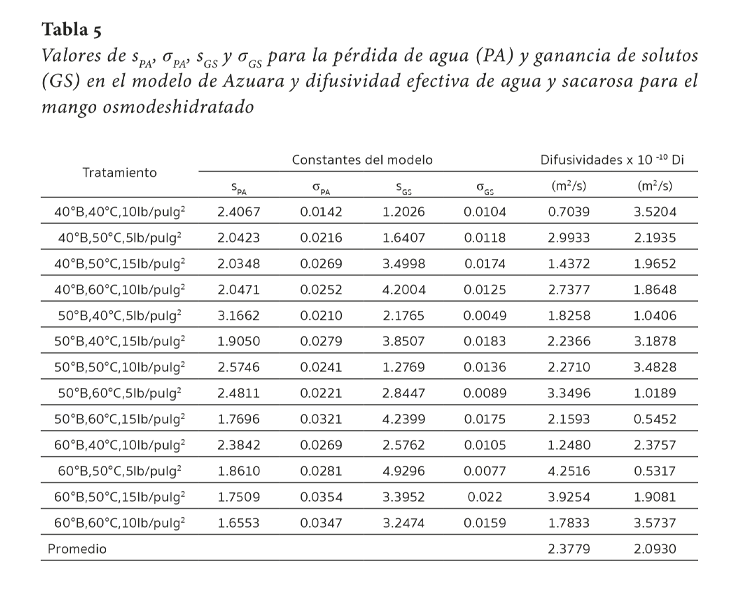
El modelo de Azuara permitió un mejor ajuste de los resultados que las ecuaciones obtenidas con la metodología de superficie de respuesta. Los parámetros sPA y sGS (Tabla 5) fueron identificados para cada una de las cinéticas con la ayuda de las ecuaciones 4, 5 y 6 y los valores encontrados estuvieron entre 1.6553 y 3.1662 para la pérdida de agua y entre 1.2026 y 4.9296 para la ganancia de solutos.
La difusividad efectiva promedio (Di), calculada con la ecuación 6, muestra que, para el caso del agua, los valores variaron entre 4.2516 x 10-10 y 0.7039 x 10-10 m2/s; mientras que para la ganancia de solutos, la Di cambió entre 3.5737 x 10-10 y 0.5317 x 10-10 m2/s. Estos valores son estadísticamente iguales por lo que calculamos un promedio de 2.3779 x 10-10 m2/s y 2.0930 x 10-10 m2/s para difusividades de agua y de sacarosa, respectivamente. Estos valores de difusividad son semejantes a los reportados por D´Aquino de los Santos et al. (2022) para la DO de papaya y Wang et al. (2021) para mango. Estos valores son también comparables a los reportados por Ayala-Aponte et al. (2018) quienes reportaron la difusividad efectiva para el agua y el cloruro de sodio impregnado en mango verde var. Filipino con valores del orden de 10-10 m2/s. Atares et al. (2009) quienes encontraron que la difusividad efectiva de agua para manzana fue de 1.53 x 10-10 m2/s y para sacarosa de 1.05 x 10-10 m2/s. Las difusividades reportadas en este trabajo resultaron superiores a las reportadas para mango var. Kent y manzana, respectivamente, para el caso de la difusividad efectiva del agua. En el caso de la difusividad efectiva del agua en papaya, esta fue aproximadamente 5 veces mayor respectivamente, y aproximadamente de 8 veces mayor para la difusividad efectiva de sacarosa en DO de papaya.
Implicaciones del estudio para la industria y futuras investigaciones
Este estudio establece las bases tecnológicas para el procesamiento industrial del mango variedad Oro, con el objetivo de extender su vida útil y diversificar su presentación comercial. Se evaluó la viabilidad de aplicar deshidratación osmótica utilizando una solución de sacarosa a 50 °Brix y una temperatura de 50 °C, sin la implementación de pulso de vacío. Bajo estas condiciones, se obtuvo un producto con menor contenido de humedad y una aceptación sensorial global favorable por parte del panel de evaluación.
El presente trabajo exploró el potencial del secado osmótico como alternativa de conservación para el mango var. Oro. No obstante, se reconoce la necesidad de continuar con estudios complementarios que permitan determinar la vida útil en anaquel de los productos obtenidos. Asimismo, se propone como línea de investigación futura el desarrollo de orejones de mango mediante la combinación de secado osmótico y secado por aire caliente, con la finalidad de optimizar la estabilidad del producto y ampliar su valor agregado en el mercado.
Conclusión
En el estudio se demuestra que la deshidratación osmótica del mango (Mangifera indica L.) var. Oro en láminas fue afectada por la concentración y temperatura de la solución osmótica. La pérdida de agua del mango se puede maximizar utilizando una solución osmótica a 60 °Brix a 57 °C, aplicando un pulso de vacío de 5 lb/plg2; mientras que la ganancia de sólidos se puede minimizar utilizando una solución de 47 °Brix a 43 °C aplicando un pulso de vacío de 8.4 lb/plg2. La optimización permitió encontrar que es posible utilizar una solución a 53 °Brix, 51°C y un pulso de vacío de 7.65 lb/plg2 para maximizar la pérdida de agua y disminuir la ganancia de sacarosa. El análisis sensorial demostró que el mango osmodeshidratado a 50 °Brix a 60 °C, con un pulso de vacío de 15 lb/plg2 tiene la mejor aceptación (7.38). La metodología de superficie de respuesta permite obtener un modelo adecuado para predecir la pérdida de agua de mango durante la deshidratación osmótica y en menor medida la ganancia de solutos, pero el modelo de Azuara permitió calcular la difusividad efectiva del agua y de la sacarosa, ambos del orden de 10-10 m2/s durante la deshidratación osmótica de mango. 1
1 Agradecimiento: Al Tecnológico Nacional de México por el financiamiento del proyecto.
Referencias
Antonio, G. C., Azoubel, P. M., Murr, F. E. & Park, K. J. (2008). Osmotic dehydration of sweet potato (Ipomoea batatas) in ternary solutions. Ciência e Tecnologia de Alimentos, Campinas, 28(3), 696-701. https://doi.org/10.1590/S0101-20612008000300028
Arias, L., Perea, Y. & Zapata, J. E. (2017). Cinética de la transferencia de masa en la deshidratación osmótica de mango (Mangifera indica L.) var. Tommy Atkins en función de la temperatura. Información Tecnológica, 28(3), 47-58. https://doi.org/10.4067/S0718-07642017000300006
Asghari, A., Zongo, P. A, Osse, E. F., Aghajanzadeh, S., Raghavan, V. & Khalloufi, S. (2024). Review of osmotic dehydration: Promising technologies for enhancing products’ attributes, opportunities, and challenges for the food industries. Comprehensive Reviews in Food Science and Food Safety, 23:e13346. https://doi.org/10.1111/1541-4337.13346.
Ayala-Aponte, A. A., Molina-Cortés, A., & Serna-Cock, L. (2018). Osmotic dehydration of green mango samples (Mangifera indica L., Filipino Var.) in ternary solutions. Vitae, 25(1): 8-16. https://doi.org/10.17533/udea.vitae.v25n1a02
Azuara, E., Flores, E. & Beristain, C. I. (2009). Water diffusion and concentration profiles during osmodehydration and storage of apple tissue. Food Bioprocess Technology, 2, 361–367. https://doi.org/10.1007/s11947-008-0077-7
Bernardi, S., Bodini, R. B., Marcatti, B., Rodrigues Petrus, R. & Favaro-Trindade, C. S. (2009). Quality and sensorial characteristics of osmotically dehydrated mango with syrups of inverted sugar and sucrose. Scientia Agricola, 66(1), 40–43. https://doi.org/10.1590/S0103-90162009000100005
D´Aquino de los Santos, C. M., Luján Hidalgo, M. C., Ventura Canseco, L. M. C. & Abud Archila, M. (2023). Deshidratación osmótica de Carica papaya var. Maradol: Transferencia de masa y análisis sensorial. Espacio I+D, Innovación más Desarrollo, 11(31). https://doi.org/10.31644/IMASD.31.2022.a08
Gomes-Corrêa, J. L., Ernesto, D. B. & Mendonça, K. S. (2016). Pulsed vacuum osmotic dehydration of tomatoes: Sodium incorporation reduction and kinetics modeling. LWT - Food Science and Technology, 71, 17-24. https://doi.org/10.1016/j.lwt.2016.01.046
Grajales-Lagunes, A., Cabrera-Ruiz, L., Gutiérrez-Miceli, F., Ruiz-Cabrera, M. A., Dendooven, L. & Abud-Archila, M. (2019). Anthocyanins from blackberry (Rubus fructicosus L.) impregnated in yam bean (Pachyrhizus erosus (L.) Urb.) by osmotic dehydration. Food Science and Technology, 39(4), 922-929. https://doi.org/10.1590/fst.15618
Huerta-Vera, K., Flores-Andrade, E., Contreras-Oliva, A., Villegas-Monter, A., Chavez-Franco, S. & Arévalo-Galarza, M. L. (2024). Incorporación de compuestos bioactivos en productos hortofrutícolas mediante deshidratación osmótica: Una revisión». Revista Mexicana De Ciencias Agrícolas, 14 (8). México, ME:e2936. https://doi.org/10.29312/remexca.v14i8.2936.
Jarry-Bolduc, G., & Planiden, C. (2025). Using generalized simplex methods to approximate derivatives, IMA Journal of Numerical Analysis, draf053, https://doi.org/10.1093/imanum/draf053
Kilic, M., Sahin, M., Hassan, A. & Ullah, A. (2024). Preservation of fruits through drying—A comprehensive review of experiments and modeling approaches. Journal of Food Process Engineering, 47:e14568. https://doi.org/10.1111/jfpe.14568
Lin, X., Luo, C. & Chen, Y. (2016). Effects of vacuum impregnation with sucrose solution on mango tissue. Journal of Food Science, 81, E1412–E1418. https://doi.org/10.1111/
1750-3841.13309.
Mari, A., Andriotis, P., Drosou, C., Laina, K.-T., Panagiotou, N. & Krokida, M. (2025). Enhancing shelf-life stability of refrigerated potatoes through osmotic dehydration and ohmic heating optimization: A strategy to mitigate enzymatic browning. Potato Research, 68: 2085–2123. https://doi.org/10.1007/s11540-024-09805-1
Mújica-Paz, H., Valdez-Fragoso, A., Lopez-Malo, A., Palou, E. & Welti-Chanes, J. (2003). Impregnation and osmotic dehydration of some fruits: effect of the vacuum pressure and syrup concentration. Journal of Food Engineering, 57, 305-314. https://doi.org/10.1016/S0260-8774(02)00344-8
Sablani, S. S. & Rahman, M. S. (2003). Effect of syrup concentration, temperature and sample geometry on equilibrium distribution coefficients during osmotic dehydration of mango. Food Research International, 36(1), 65-71. https://doi.org/10.1016/S0963-9969(02)00109-6
SAGARPA (2017). Planeación agrícola nacional 2017 – 2030, https://www.gob.mx/cms/uploads/attachment/file/257078/Potencial-Mango.pdf
Sanjinez-Argandoña, E. J., Yahagi, L. Y., Boveda Costa, T. & Giunco, A. J. (2017). Mango dehydration: influence of osmotic pre-treatment and addition of calcium chloride. Revista Brasileira de ruticultura, 40(4): e-419. http://dx.doi.org /10.1590/0100-29452018419
Smattcom (2024). El mango mexicano: Un tesoro comercial en 2024. https://smattcom.com/blog/mango-mexicano-tesoro-comercial-2024
Staniszewska, I., Nowak, K. W., Zielinska, D., Konopka, I. & Zielinska, M. (2024). Pulsed vacuum osmotic dehydration (PVOD) of fermented beetroot: modeling and optimization by Response Surface Methodology (RSM). Food and Bioprocess Technology, 17: 977–990. https://doi.org/10.1007/s11947-023-03173-3
Sulistyawati, I., Dekker, M., Fogliano, V. & Verkerk, R. (2018). Osmotic dehydration of mango: Effect of vacuum impregnation, high pressure, pectin methylesterase and ripeness on quality. LWT-Food Science and Technology, 98: 179-186. https://doi.org/10.1016/j.lwt.2018.08.032
Sulistyawati, I., Verkerk, R., Fogliano, V. & Dekker, M. (2020). Modelling the kinetics of osmotic dehydration of mango: Optimizing process conditions and pre-treatment for health aspects. Journal of Food Engineering, 280: 109985, https://doi.org/10.1016/j.jfoodeng.2020.109985
Tsopwo Zena, C. y Jiokap Nono. (2024). Investigating intermittent immersion during osmotic dehydration of mango (Mangifera indica L. Moench). Part A: Determination of optimal conditions for mango (Mangifera indica L. Moench) dehydration impregnation by immersion (D2I) and intermittent immersion (D3I). Heliyon, 10(16): e35808. https://www.cell.com/heliyon/fulltext/S2405-8440(24)11839-7
Vinod, B.R., Asrey, R., Sethi, S., Menaka, M., Meena, N. K. & Shivaswamy, G. (2024). Recent advances in vacuum impregnation of fruits and vegetables processing: A concise review, Heliyon, 10, e28023. https://doi.org/10.1016/j.heliyon.2024.e28023
Wang, J., Teng, J., Wei, B., Huang, L., & Xia, N. (2021). Effects of different osmosis methods on the dehydration efficiency and quality of mango fruits. Food Science, 42(1), 149–156. https://doi.org/10.7506/spkx1002-6630-20191110-127
Zapata Montoya, J.E. & Montoya Ramos, A. (2012). Deshidratación osmótica de láminas de mango cv. Tommy Atkins aplicando metodología de superficies de respuesta. Revista Facultad Nacional de Agronomía Medellín, 65(1): 6507-6518. (PDF) Osmotic Dehydration of Mango Pieces cv. Tommy Atkins Applying Response Surface Methodology
 https://orcid.org/0000-0003-0572-8845
https://orcid.org/0000-0003-0572-8845
 https://orcid.org/0000-0003-0418-1315
https://orcid.org/0000-0003-0418-1315
 https://orcid.org/0000-0003-0983-3247
https://orcid.org/0000-0003-0983-3247
 https://orcid.org/0000-0002-4509-7964
https://orcid.org/0000-0002-4509-7964